Hidrojen bağı
Kimya'da, hidrojen bağı (veya H-bağı) öncelikle daha elektronegatif bir "verici" atom veya gruba (Dn) kovalent bağla bağlanan bir hidrojen (H) atomu ile ve yalnız bir çift elektron taşıyan başka bir elektronegatif atom (hidrojen bağı alıcısı (Ac)) arasındaki elektrostatik çekim kuvvetidir.
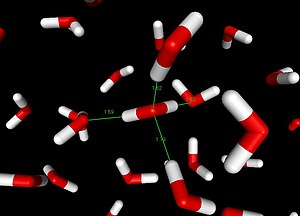


Böyle etkileşimli bir sistem genel olarak Dn−H···Ac olarak gösterilir ki burada düz çizgi polar kovalent bağ'ı ve noktalı veya kesikli çizgi ise hidrojen bağını belirtir.[5] En sık görülen verici ve alıcı atomlar 2. periyot elementleri azot (N), oksijen (O) ve flor (F)'dur. Genelde bağ, hidrojenin flor, oksijen ve azot gibi elektronegatifliği yüksek atomlarla yapmış olduğu kuvvetli bir etkileşim türüdür.
Hidrojen bağları moleküller arası (ayrı moleküller arasında oluşabilir) veya molekül içi (aynı molekülün parçaları arasında) olabilir.[6][7][8] Hidrojen bağının enerjisi geometriye, çevreye ve belirli verici ve alıcı atomların doğasına bağlıdır ve 1 ila 40 kcal/mol arasında değişebilir.[9] Bu onları van der Waals etkileşiminden biraz daha güçlü, tam kovalent veya iyonik bağlardan ise daha zayıf kılar. Hidrojen bağı, su gibi inorganik moleküllerde ve DNA ve proteinler gibi organik moleküllerde meydana gelebilir. Hidrojen bağları, kâğıt ve keçeli yün gibi malzemeleri bir arada tutar ve ayrı kağıt yapraklarının ıslanıp kuruduktan sonra birbirine yapışmasını sağlar.
Hidrojen bağı aynı zamanda N, O ve F bileşiklerinin diğer benzer yapılarla karşılaştırıldığında sıra dışı görünen birçok fiziksel ve kimyasal özelliğinden de sorumludur. Özellikle moleküller arası hidrojen bağı, çok daha zayıf hidrojen bağlarına sahip olan diğer grup-16 hidritlere kıyasla suyun yüksek kaynama noktasından (100 °C) sorumludur.[10] Molekül içi hidrojen bağı, proteinlerin ve nükleik asitlerin ikincil ve üçüncül yapılarından kısmen sorumludur.
Proteinler ve nükleik asitler gibi makromoleküller içinde, aynı molekülün iki parçası arasında var olabilir.
Hidrojen bağı ismi, bağın bir hidrojen atomunu kapsamasından gelir.
Eğer hidrojen bağı atomu iki atom arasında ortak kullanılıyor ise meydana gelen iki molekül arasındaki zayıf bir bağdır.
Hidrojen bağları genellikle oksijen ve azot gibi negatif elektrik yüklü atomlarla diğer bir negatif yüklü atomlara kovalent olarak bağlanmış hidrojen atomları arasında oluşan bağlardır.
Dipol dipol etkileşmesinin kimyadaki en bariz örneğidir.
Hidrojen Bağı Van der Waals bağından güçlüdür, molekülleri arasında daha güçlü etkileşim olan maddenin kaynama noktası daha yüksektir.Bu yüzden hidrojen bağı içeren maddelerin erime - kaynama noktaları Van der Waals bağı içeren maddelere göre daha yüksektir.
İki farklı molekül birbirleriyle hidrojen bağı oluşturabilir.
(F,O,N) barındıran moleküller dışında hidrojen sülfürün de (H₂S) bağ yapabildiği keşfedilmiştir.
Bağlanma
değiştirTanımlar ve genel özellikler
değiştirBir hidrojen bağında, hidrojene kovalent olarak bağlanmayan elektronegatif atom, proton alıcısı olarak adlandırılırken, hidrojene kovalent olarak bağlanan atom, proton donörü olarak adlandırılır. Bu terminoloji IUPAC tarafından tavsiye edilmektedir.[5] Vericinin hidrojeni protiktir ve bu nedenle bir Lewis asidi gibi davranabilir ve alıcı ise Lewis bazıdır. Hidrojen bağları H···Y sistemi olarak temsil edilir ki burada noktalar hidrojen bağını temsil eder. Hidrojen bağı sergileyen sıvılara (su gibi) ilişkili sıvılar denir.
Hidrojen bağları, elektrostatiklerin (çok kutuplu-çok kutuplu ve çok kutuplu- kaynaklı çok kutuplu etkileşimler), kovalans (yörünge örtüşmesiyle yük aktarımı) ve dispersiyonun (London kuvvetleri) birleşiminden kaynaklanır.[5]
Daha zayıf hidrojen bağlarında,[12] hidrojen atomları kükürt (S) veya klor (Cl) gibi elementlere bağlanma eğilimindedir; karbon (C) bile, özellikle karbon veya komşularından biri elektronegatif olduğunda (örneğin, kloroform, aldehitler ve terminal asetilenlerde) bir donör görevi görebilir.[13][14] Yavaş yavaş, N, O veya F dışındaki donörleri ve/veya elektronegatifliği hidrojeninkine yaklaşan (çok daha elektronegatif olmak yerine) alıcı Ac'yi içeren daha zayıf hidrojen bağının birçok örneğinin olduğu fark edildi. Her ne kadar zayıf (≈1 kcal/mol) olsa da, "geleneksel olmayan" hidrojen bağı etkileşimleri her yerde bulunur ve birçok türde malzemenin yapısını etkiler.
Hidrojen bağının tanımı zamanla bu daha zayıf çekici etkileşimleri içerecek şekilde kademeli olarak genişletildi. 2011 yılında bir IUPAC Görev Grubu, IUPAC Pure and Applied Chemistry dergisinde yayınlanan, hidrojen bağının modern, kanıta dayalı bir tanımını önerdi. Bu tanım şöyledir:
Hidrojen bağı, X'in H'den daha elektronegatif olduğu bir molekülden veya bir moleküler parçadan (X−H) gelen bir hidrojen atomu ile aynı veya başka bir moleküldeki bağ oluşumuna dair kanıtların bulunduğu bir atom veya atom grubu arasındaki çekici bir etkileşimdir.[15]
Bağ kuvveti
değiştirHidrojen bağlarının gücü zayıftan (1–2 kJ/mol) güçlüye (biflorür iyonunda 161,5 kJ/mol, HF−
2) kadar değişebilir.[16][17] Buhardaki tipik entalpiler şunları içerir:[18]
- F−H···:F−
(161.5 kJ/mol veya 38.6 kcal/mol), illustrated uniquely by HF−
2 - O−H···:N (29 kJ/mol veya 6.9 kcal/mol), resimli su-amonyak
- O−H···:O (21 kJ/mol veya 5.0 kcal/mol), resimli su-su, alkol-alkol
- N−H···:N (13 kJ/mol veya 3.1 kcal/mol), resimli amonyak-amonyak ile gösterilmiştir
- N−H···:O (8 kJ/mol or 1.9 kcal/mol), resimli su-amid
- OH+
3···:OH
2 (18 kJ/mol[19] veya 4.3 kcal/mol)
Moleküller arası hidrojen bağlarının gücü çoğunlukla donör ve/veya alıcı birimleri içeren moleküller arasındaki denge ölçümleriyle değerlendirilir; çoğunlukla çözelti içindedir.[20] Molekül içi hidrojen bağlarının gücü, hidrojen bağı olan ve olmayan konformerler arasındaki denge ile incelenebilir. Karmaşık moleküllerde de hidrojen bağlarının tanımlanmasına yönelik en önemli yöntem kristalografi, bazen de NMR-spektroskopidir. Van der Waals yarıçaplarının toplamından daha küçük olan donör ve alıcı arasındaki mesafeler gibi yapısal ayrıntılar, hidrojen bağı kuvvetinin göstergesi olarak alınabilir. Bir şema aşağıdaki biraz keyfi sınıflandırmayı verir: 15 ila 40 kcal/mol, 5 ila 15 kcal/mol ve >0 ila 5 kcal/mol olanlar sırasıyla güçlü, orta ve zayıf olarak kabul edilir.[17]
C-H bağlarını içeren hidrojen bağları hem çok nadir hem de zayıftır.[21]
Kaynakça
değiştir- ^ Sweetman, A. M.; Jarvis, S. P.; Sang, Hongqian; Lekkas, I.; Rahe, P.; Wang, Yu; Wang, Jianbo; Champness, N.R.; Kantorovich, L.; Moriarty, P. (2014). "Mapping the force field of a hydrogen-bonded assembly". Nature Communications. Cilt 5. s. 3931. Bibcode:2014NatCo...5.3931S. doi:10.1038/ncomms4931. PMC 4050271 $2. PMID 24875276.
- ^ Hapala, Prokop; Kichin, Georgy; Wagner, Christian; Tautz, F. Stefan; Temirov, Ruslan; Jelínek, Pavel (19 Ağustos 2014). "Mechanism of high-resolution STM/AFM imaging with functionalized tips". Physical Review B. 90 (8). s. 085421. arXiv:1406.3562 $2. Bibcode:2014PhRvB..90h5421H. doi:10.1103/PhysRevB.90.085421.
- ^ De Luca, S.; Chen, F.; Seal, P.; Stenzel, M. H.; Smith, S. C. (2017). "Binding and Release between Polymeric Carrier and Protein Drug: pH-Mediated Interplay of Coulomb Forces, Hydrogen Bonding, van der Waals Interactions, and Entropy". Biomacromolecules. 18 (11). ss. 3665-3677. doi:10.1021/acs.biomac.7b00657. PMID 28880549.
- ^ Hämäläinen, Sampsa K.; van der Heijden, Nadine; van der Lit, Joost; den Hartog, Stephan; Liljeroth, Peter; Swart, Ingmar (31 Ekim 2014). "Intermolecular Contrast in Atomic Force Microscopy Images without Intermolecular Bonds". Physical Review Letters. 113 (18). s. 186102. arXiv:1410.1933 $2. Bibcode:2014PhRvL.113r6102H. doi:10.1103/PhysRevLett.113.186102. hdl:1874/307996. PMID 25396382. 20 Ocak 2018 tarihinde kaynağından arşivlendi. Erişim tarihi: 30 Ağustos 2017.
- ^ a b c Arunan, Elangannan; Desiraju, Gautam R.; Klein, Roger A.; Sadlej, Joanna; Scheiner, Steve; Alkorta, Ibon; Clary, David C.; Crabtree, Robert H.; Dannenberg, Joseph J. (8 Temmuz 2011). "Definition of the hydrogen bond (IUPAC Recommendations 2011)". Pure and Applied Chemistry. 83 (8). ss. 1637-1641. doi:10.1351/PAC-REC-10-01-02. ISSN 1365-3075.
- ^ Pimentel, G. The Hydrogen Bond Franklin Classics, 2018), 0343171600
- ^ Jeffrey, G. A.; An introduction to hydrogen bonding; Oxford university press New York, 1997. 0195095499
- ^ Jeffrey, G. A.; Saenger, W. Hydrogen bonding in biological structures; Springer: Berlin, 1994, 2012 Springer; 3540579036
- ^ Steiner, Thomas (2002). "The Hydrogen Bond in the Solid State". Angew. Chem. Int. Ed. 41 (1). ss. 48-76. doi:10.1002/1521-3773(20020104)41:1<48::AID-ANIE48>3.0.CO;2-U. PMID 12491444.
- ^ Sabin, John R. (1971). "Hydrogen bonds involving sulfur. I. Hydrogen sulfide dimer". J. Am. Chem. Soc. 93 (15). ss. 3613-3620. doi:10.1021/ja00744a012.
- ^ Beijer, Felix H.; Kooijman, Huub; Spek, Anthony L.; Sijbesma, Rint P.; Meijer, E. W. (1998). "Self-Complementarity Achieved through Quadruple Hydrogen Bonding". Angew. Chem. Int. Ed. 37 (1–2). ss. 75-78. doi:10.1002/(SICI)1521-3773(19980202)37:1/2<75::AID-ANIE75>3.0.CO;2-R.
- ^ Desiraju, G. R. and Steiner, T. The Weak Hydrogen Bond: In Structural Chemistry and Biology, International Union of Crystallography;2001, 0198509707
- ^ Nishio, M.; Hirota, M.; Umezawa, Y. The CH–π Interactions; Wiley-VCH, New York, 1998. • Wiley-VCH; 1998) 0471252905
- ^ Nishio, M (2011). "The CH/[small pi] hydrogen bond in chemistry. "Title". Phys. Chem. Chem. Phys. 13 (31). ss. 13873-13900. doi:10.1039/c1cp20404a. PMID 21611676.
- ^ Arunan, Elangannan; Desiraju, Gautam R.; Klein, Roger A.; Sadlej, Joanna; Scheiner, Steve; Alkorta, Ibon; Clary, David C.; Crabtree, Robert H.; Dannenberg, Joseph J.; Hobza, Pavel; Kjaergaard, Henrik G.; Legon, Anthony C.; Mennucci, Benedetta; Nesbitt, David J. (2011). "Definition of the hydrogen bond". Pure Appl. Chem. 83 (8). ss. 1637-1641. doi:10.1351/PAC-REC-10-01-02.
- ^ Larson, J. W.; McMahon, T. B. (1984). "Gas-phase bihalide and pseudobihalide ions. An ion cyclotron resonance determination of hydrogen bond energies in XHY- species (X, Y = F, Cl, Br, CN)". Inorganic Chemistry. 23 (14). ss. 2029-2033. doi:10.1021/ic00182a010.
- ^ a b Emsley, J. (1980). "Very Strong Hydrogen Bonds". Chemical Society Reviews. 9 (1). ss. 91-124. doi:10.1039/cs9800900091.
- ^ V. David, N. Grinberg, S. C. Moldoveanu in Advances in Chromatography Volume 54 (Eds.: E. Grushka, N. Grinberg), CRC Press, Boca Raton, 2018, chapter 3.
- ^ Referansta ayrıntılı olarak açıklandığı gibi moleküler dinamik kullanılarak elde edilen veriler, aynı hesaplama kullanılarak elde edilen toplu su için 7,9 kJ/mol ile karşılaştırılmalıdır.Markovitch, Omer; Agmon, Noam (2007). "Structure and energetics of the hydronium hydration shells" (PDF). The Journal of Physical Chemistry A. 111 (12). ss. 2253-2256. Bibcode:2007JPCA..111.2253M. CiteSeerX 10.1.1.76.9448 $2. doi:10.1021/jp068960g. PMID 17388314. 13 Ağustos 2014 tarihinde kaynağından (PDF) arşivlendi. Erişim tarihi: 25 Ekim 2017.
- ^ Biedermann F, Schneider HJ (Mayıs 2016). "Experimental Binding Energies in Supramolecular Complexes". Chemical Reviews. 116 (9). ss. 5216-300. doi:10.1021/acs.chemrev.5b00583. PMID 27136957.
- ^ Gu, Yanliang; Kar, Tapas; Scheiner, Steve (1999). "Fundamental Properties of the CH···O Interaction: Is It a True Hydrogen Bond?". Journal of the American Chemical Society. 121 (40). ss. 9411-9422. doi:10.1021/ja991795g.
| Fiziksel kimya ile ilgili bu madde taslak seviyesindedir. Madde içeriğini genişleterek Vikipedi'ye katkı sağlayabilirsiniz. |