Nitrozilsülfürik asit
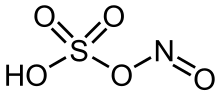
Nitrozilsülfürik asit, NOHSO4 formülüne sahip bir kimyasal bileşiktir. Endüstriyel olarak kaprolaktam üretiminde kullanılan renksiz bir katıdır.[1] Daha önce sülfürik asit üretmek için öncü oda işleminin bir parçasıydı. Bileşik, sülfürik asit ve nitröz asidin karışık anhidritidir.
| |

| |
Diğer adlar Nitrosonyum bisülfat | |
| Tanımlayıcılar | |
|---|---|
3D model (JSmol)
|
|
| ChemSpider | |
| ECHA InfoCard | 100.029.058 |
PubChem CID
|
|
CompTox Bilgi Panosu (EPA)
|
|
| |
| Özellikler | |
| Molekül formülü | HNO5S |
| Molekül kütlesi | 127.08 g/mol |
| Görünüm | Soluk sarı kristal |
| Yoğunluk | 1.612 g/mL (%40 sülfürik asit çözeltisinde) |
| Erime noktası | 70 °C (158 °F |
| Kaynama noktası | Ayrışır |
| Çözünürlük (su içinde) | Ayrışır |
| Çözünürlük | H2SO4 içinde ayrışır |
| Tehlikeler | |
| İş sağlığı ve güvenliği (OHS/OSH): | |
| Ana tehlikeler | Oksitleyici |
| Aksi belirtilmediği sürece madde verileri, Standart sıcaklık ve basınç koşullarında belirtilir (25 °C [77 °F], 100 kPa).
| |
| Bilgi kutusu kaynakları | |
Organik kimyada, nitrozlama için bir reaktif olarak, bir diazotize edici ajan olarak ve bir oksitleyici ajan olarak kullanılır.[2]
Sentezi ve tepkimeler
değiştirTipik bir prosedür sodyum nitritin soğuk sülfürik asit içinde çözülmesini gerektirir:[3][4]
- HNO2 + H2SO4 → NOHSO4 + H2O
Ayrıca nitrik asit ve sülfür dioksit reaksiyonu ile hazırlanabilir.[5]
NOHSO4 organik kimyada aminlerden diazonyum tuzları hazırlamak için, örneğin Sandmeyer reaksiyonunda kullanılır. İlgili NO-dağıtım reaktifleri arasında nitrosonyum tetrafloroborat ([NO]BF4) ve nitrozil klorür yer alır.
Güvenlik
değiştirNitrozilsülfürik asit tehlikeli bir maddedir ve önlemler belirtilir.[2]
Kaynakça
değiştir- ^ Ritz, J.; Fuchs, H.; Kieczka, H.; Moran, W. C. (2002). "Caprolactam". Ullmann's Encyclopedia of Industrial Chemistry. Ullmann's Encyclopedia of Industrial Chemistry. Weinheim: Wiley-VCH. doi:10.1002/14356007.a05_031. ISBN 978-3527306732.
- ^ a b George A. Olah, G. K. Surya Prakash, Qi Wang, Xing-Ya Li (2001). Nitrosylsulfuric Acid. E-EROS Encyclopedia of Reagents for Organic Synthesis. doi:10.1002/047084289X.rn060. ISBN 978-0471936237.
- ^ Hodgson, H. H.; Mahadevan, A. P.; Ward, E. R. (1955). "1,4-Dinitronaphthalene" 9 Haziran 2019 tarihinde Wayback Machine sitesinde arşivlendi.. Organic Syntheses.; Collective Volume, 3, p. 341 (diazodization followed by treatment with nitrite)
- ^ Sandin, R. B.; Cairns, T. L. (1943). "1,2,3-Triiodo-5-nitrobenzene" 5 Haziran 2019 tarihinde Wayback Machine sitesinde arşivlendi.. Organic Syntheses.; Collective Volume, 2, p. 604 (diazodization followed by treatment with iodide)
- ^ Coleman, G. H.; Lillis, G. A.; Goheen, G. E. (1939). Nitrosyl Chloride. Inorganic Syntheses. 1. pp. 55–59. doi:10.1002/9780470132326.ch20. ISBN 9780470132326. This procedure generates the nitrosylsulfuric acid as an intermediate en route to NOCl.